摩方精密圣地亚哥研究院《Bioengineering》:突破性仿生三维可灌注血管化皮肤芯片研发成功,开启药物与化妆品测试新时代
发布日期:2024-11-01
浏览量:2034次
自2013年欧盟全面禁止化妆品动物实验以来,体外重建皮肤模型已广泛应用于药物和化妆品功效研究及毒理评价。然而,现有的体外皮肤模型在模拟皮肤功能方面,尤其在血管化重建方面,仍存在显著不足,这导致难以实现组织区域的有效灌注。
摩方精密圣地亚哥研究院团队开发了一种全新的三维可灌注血管化皮肤芯片,采用了摩方精密的面投影微立体光刻(PμSL)技术,精确构建仿生微毛细血管网络系统。该皮肤芯片在营养供给、增强屏障功能和维持组织活性方面表现卓越,与传统的内皮细胞自组装或牺牲材料方法相比,该模型简化了操作流程并提高了实验的可重复性。通过石蜡切片、苏木精-伊红(H&E)染色和免疫荧光标记方法,验证了芯片中的真皮层和表皮层的完整结构。
此外,该芯片支持高通量测试,其定制化夹具支持在多孔板中同时进行多个芯片的灌注实验。通过使用TNF-α诱导炎症及地塞米松的抗炎治疗,摩方研究团队将该芯片与传统2D培养和人类皮肤活检样本进行了对比。结果表明,皮肤芯片与人类皮肤的药物反应趋势一致,且在长期培养中表现出更低的细胞毒性。这一灌注皮肤芯片为药物和化妆品筛选提供了一个高度仿生的体外模型,显著提高了实验的生理相关性。
01精密3D打印与微流控设计,还原真实血管化全层皮肤环境
通过PμSL 3D打印技术(microArch® S230,精度:2微米),摩方研究团队成功地在芯片中构建了仿生微毛细血管网络系统。该系统中,每个中空的微通道表面均匀分布有7微米的开放微孔,微通道内可以灌输细胞培养基,使得营养物质和氧气能够从通道内均匀扩散至管道外的细胞培养区域。同时,灌输系统可有效排出代谢废物,从而确保细胞的健康生长和组织的长期活性。微通道贯穿整个皮肤组织,保证了培养基在组织内的均匀供给。

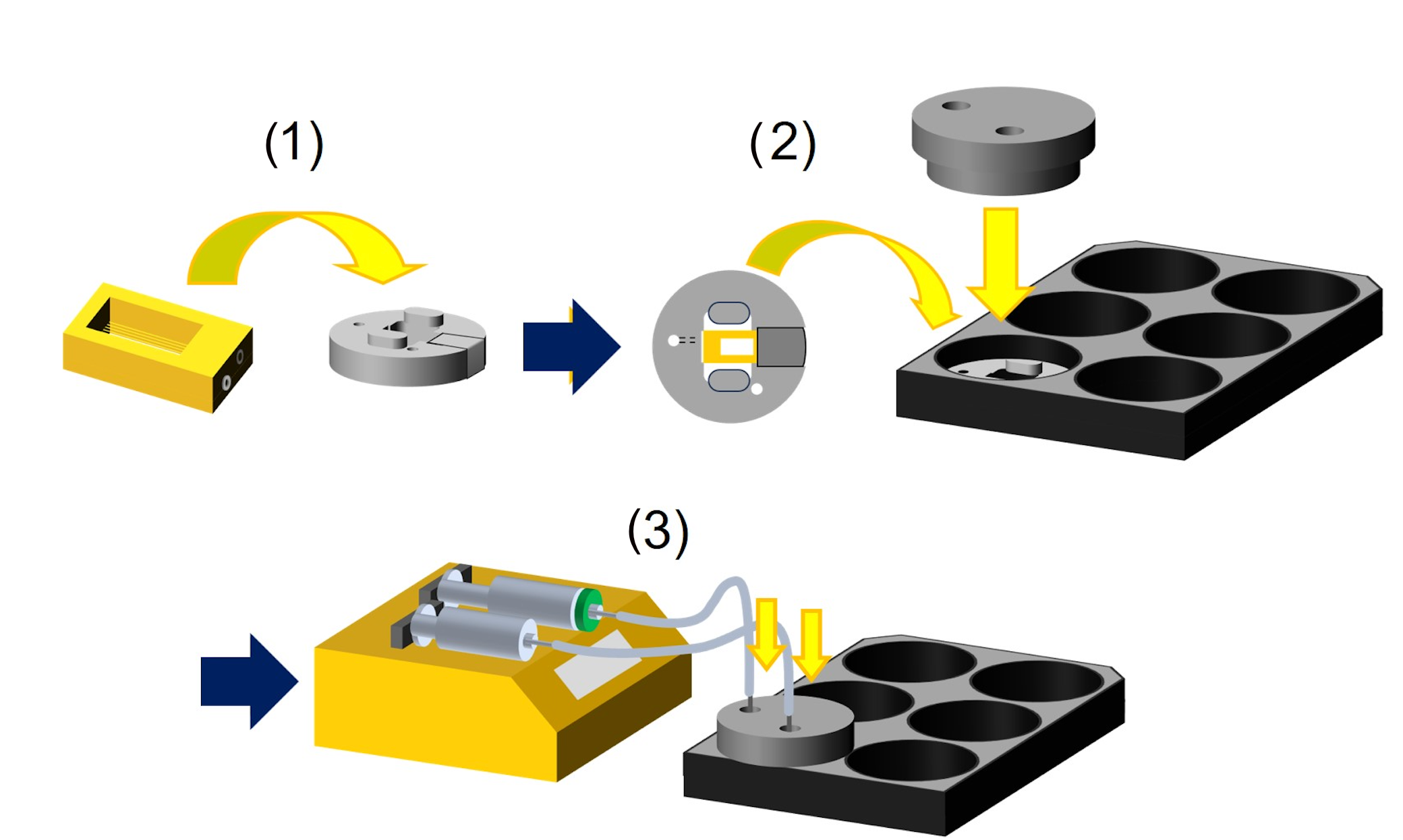
图1. 皮肤芯片与夹具示意图。(a,b) 皮肤芯片的俯视图与正视图,显示微通道的布局及内部结构;(c) 微孔的扫描电镜(SEM)图像,比例尺:200微米;(d) 放大后的SEM图像,展示单个微孔,比例尺:20微米;(e) 皮肤芯片与夹具组装前的图像;(f) 皮肤芯片装入夹具后的侧视图;(g) 六个皮肤芯片及夹具放置于六孔板中的图像。
02灌注监测流体情况,营养供给和小分子吸收测试
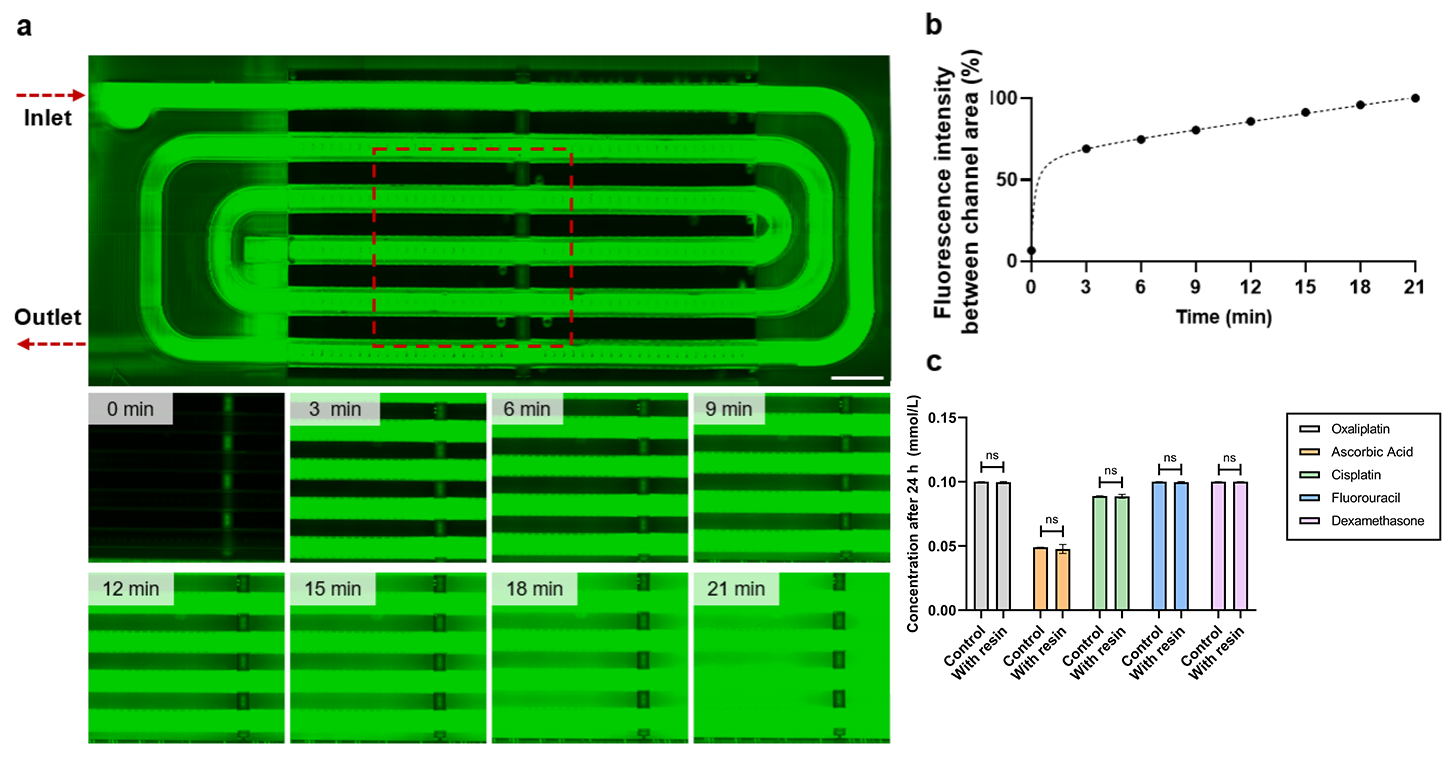
研究团队使用荧光小分子溶液进行灌注测试,监测流体在芯片中的流动与扩散情况。荧光溶液以10微升/分钟的速度注入微通道,荧光分子均匀扩散并充满芯片,整块芯片中的荧光强度随之而逐渐增加(图3a-b)。虽然PDMS常用于传统器官芯片系统,但其对小分子的吸收会影响药物测试的准确性。因此,研究团队对芯片使用的BIO材料进行了小分子药物的吸收测试,将五种FDA批准的小分子药物与BIO材料孵育24小时并和对照组对比,通过高效液相色谱法(HPLC)进行分析。结果表明,BIO材料中的药物浓度与对照组无显著差异,证明该材料不会吸收小分子(图3c)。
03仿真人类皮肤组织的构建,灌注系统应用及形态分析
为了模拟体内皮肤环境,研究团队在皮肤芯片上成功重建了表皮层和真皮层。真皮层由成纤维细胞与I型胶原蛋白水凝胶构成,表皮层则由种植在真皮层上的角质形成细胞组成。真皮层被种植在微通道周围,确保灌注系统能够有效地为皮肤组织提供营养供应。石蜡切片与苏木精-伊红(H&E)染色结果显示,本研究构建的皮肤模型具有清晰的表皮和真皮结构,且角质形成细胞向真皮层的迁移极少(图4)。
通过免疫染色,研究团队使用共聚焦显微镜确认了皮肤模型的组织形态。表皮层中角蛋白10(CK10)的表达和基底层中角蛋白14(CK14)的表达验证了表皮层的均匀性和结构完整性(图5a)。此外,真皮层中的成纤维细胞形态以及I型和IV型胶原蛋白的表达也得到了清晰的展示(图5b, c)。表皮层还观察到了分化标记物外皮蛋白(involucrin)和丝聚合蛋白(filaggrin)的表达(图5d, e)。
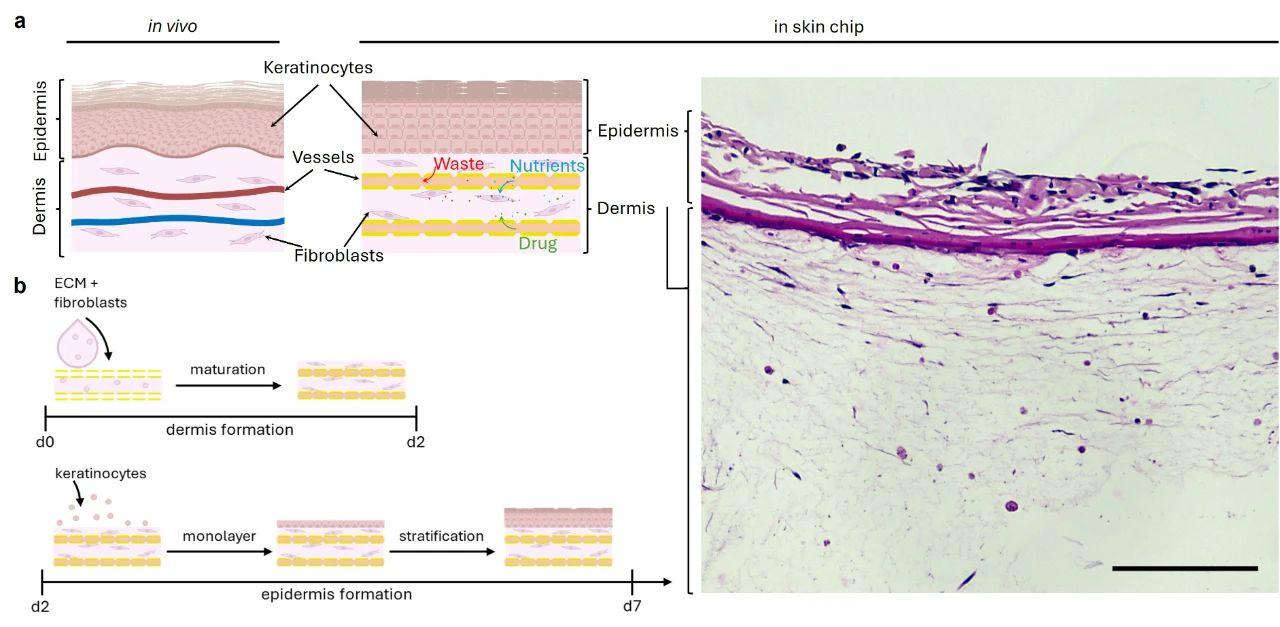
图4. 皮肤芯片中皮肤组织结构及形成的示意图。(a) 体内皮肤结构与芯片皮肤结构的对比,角质形成细胞、真皮成纤维细胞的位置以及营养物质、废物和药物的传输。右侧为皮肤芯片组织切片的苏木精-伊红(H&E)染色图像,比例尺:75微米;(b) 皮肤芯片中,从真皮形成到表皮形成的过程示意图。
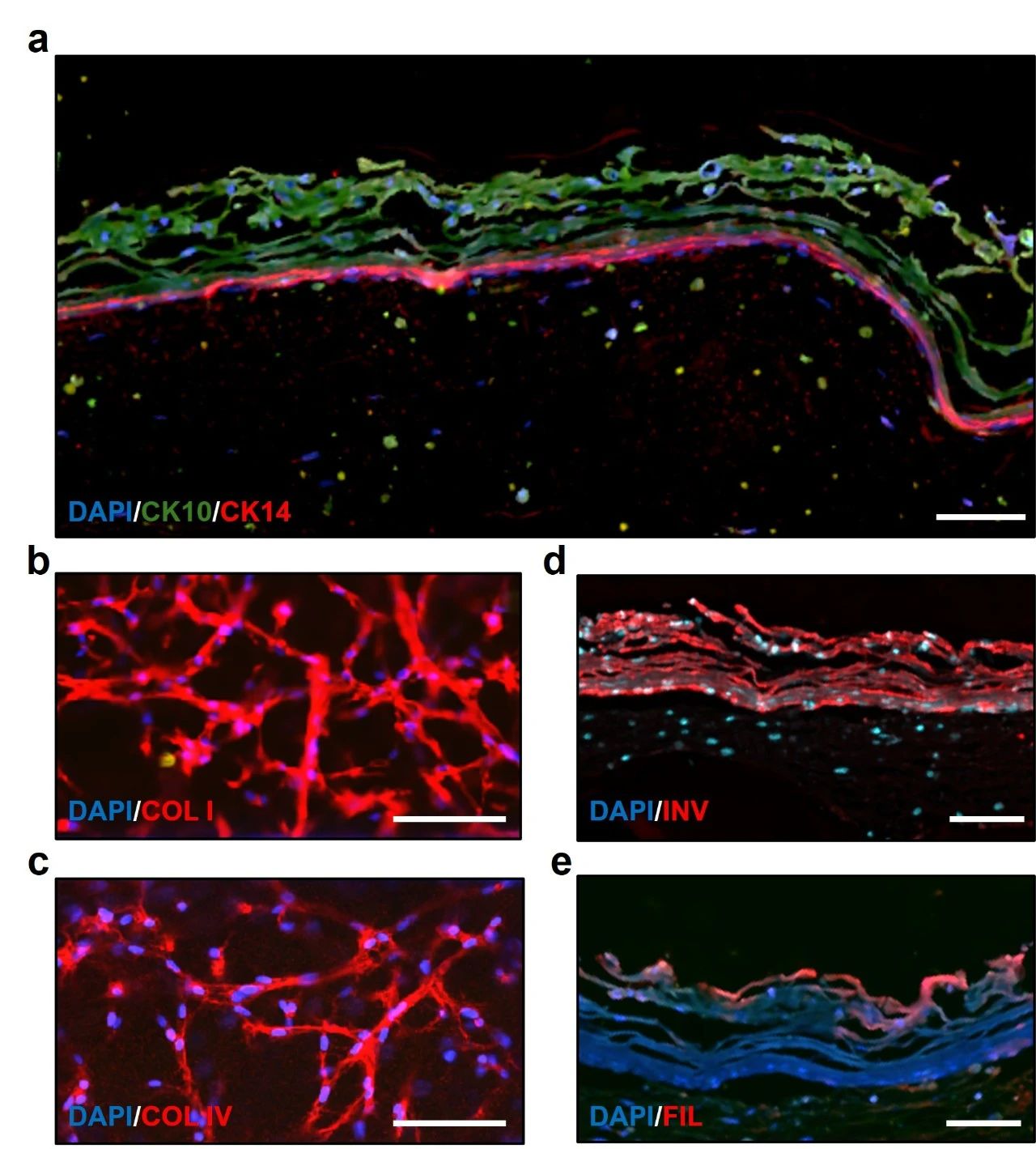
图5. 免疫荧光图像显示皮肤构建中表皮层和真皮层的存在。(a) 表皮层的横截面,显示角蛋白10和角蛋白14的表达;(b,c) 真皮层的底部视图,显示I型胶原蛋白和IV型胶原蛋白的表达;(d,e) 表皮层的横截面,显示外皮蛋白(involucrin)的表达和丝聚合蛋白(filaggrin)的表达,比例尺:75微米。
04关键应用与实验结果,皮肤芯片在药物测试中的应用
炎症是最常见的皮肤疾病之一,影响约25%的人口。为测试皮肤芯片构建炎症模型并用于药物检测的有效性,研究团队通过使用促炎细胞因子TNF-α在芯片中诱导炎症,并使用抗炎药物地塞米松进行治疗。地塞米松作为FDA批准的抗炎药物,能够有效缓解红肿、发热及疼痛。
实验设置了三种条件:对照组、炎症组和炎症+药物组。对照组使用空白培养基;炎症组于第二天加入TNF-α,24小时后更换为空白培养基;炎症+药物组于第二天加入TNF-α,24小时后更换为地塞米松。研究团队分别在各个关键时间点收集上清液,通过酶联免疫吸附试验(ELISA)检测促炎细胞因子白细胞介素-6(IL-6)和白细胞介素-8(IL-8)的表达。
为验证皮肤芯片的准确药物响应,研究团队还与2D培养的角质形成细胞和人类皮肤活检样本的药物响应情况进行了对比。2D培养模型对炎症和地塞米松的敏感性较高,在加入TNF-α后24小时内炎症急剧上升,TNF-α去除后炎症立即下降,而地塞米松的加入更加显著地降低了IL-6和IL-8的水平。相比之下,人类皮肤活检样本的反应较慢,TNF-α诱导24小时后炎症水平上升幅度较小,而在第三天去除TNF-α并换成空白培养基后,炎症组的炎症水平却持续上升;与此同时,炎症+药物组的炎症水平在第三天加入地塞米松后得到了有效控制。通过对比,皮肤芯片与人类皮肤活检的药物响应结果相似,在TNF-α诱导的过程中显示出了相对于2D 培养的延迟炎症反应,且在加入地塞米松后炎症水平得到了有效控制(图6)。
比较三种培养模型的整体趋势,人类皮肤活检样本与我们的皮肤芯片显示了相似的炎症和地塞米松治疗模式,而2D培养模型则表现出更为剧烈的炎症波动,形成了显著不同的药物响应趋势。这表明,皮肤芯片模型能够更准确地预测体内反应,从而提高药物效力与安全性评估的可靠性。
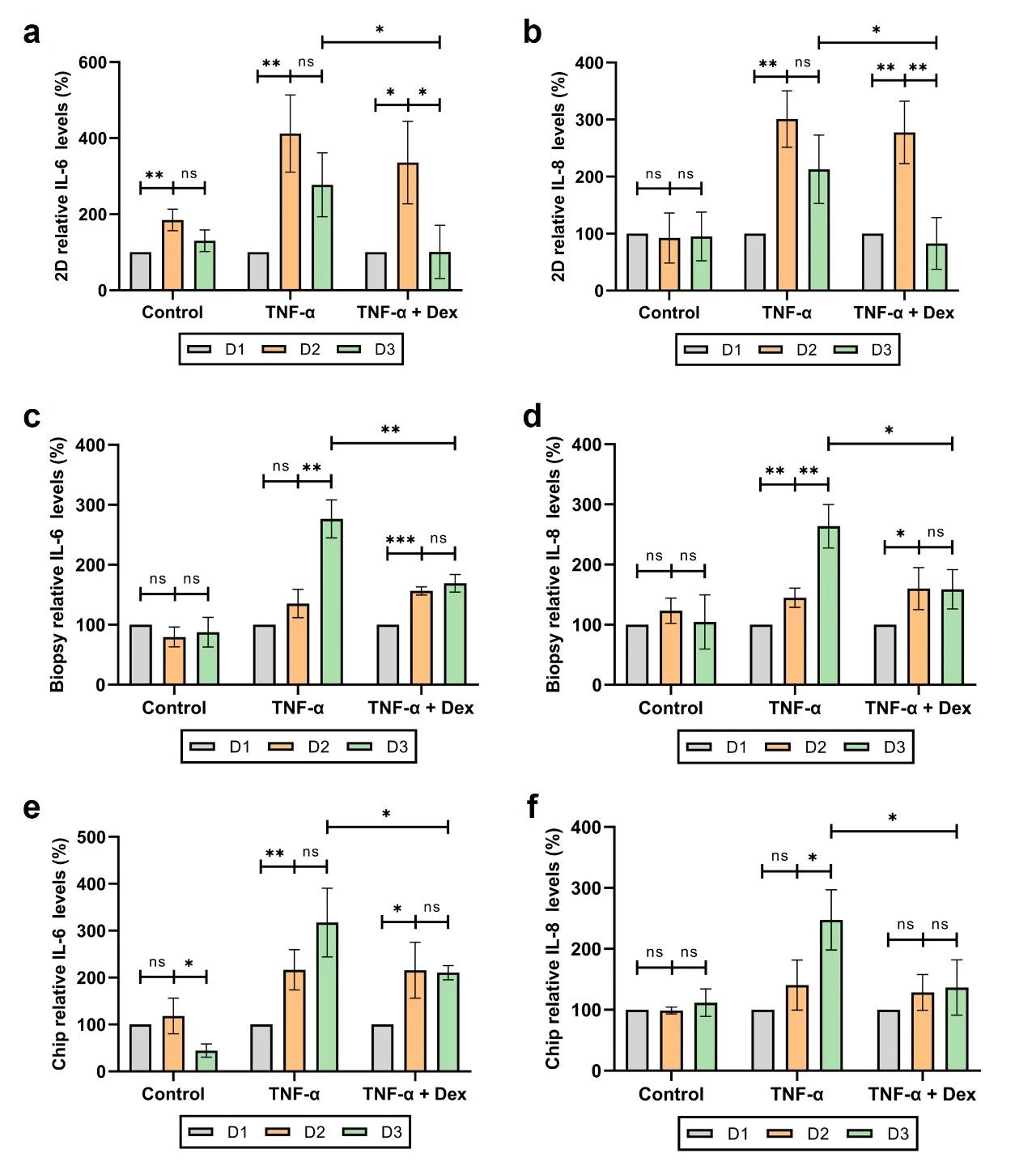
图6. 不同培养条件下的相对细胞因子水平变化。在3天的炎症诱导和药物处理后检测不同培养条件下的细胞因子水平:(a, b) 2D培养模型中的相对IL-6和IL-8水平变化;(c, d) 人类皮肤活检样本中的相对IL-6和IL-8水平变化;(e, f) 皮肤芯片中的相对IL-6和IL-8水平变化;Control:对照组;TNF-α:仅炎症组;TNF-α + Dex:炎症+药物组。
05长时间培养的细胞稳定性,实现灵活与高性能生产兼顾
皮肤活检样本在细胞活性和可培养时间上存在较大的批次差异。为评估长期培养中的细胞活性,研究团队检测了皮肤芯片、2D培养及人类皮肤活检样本上清液中乳酸脱氢酶(LDH)的表达水平。LDH是检测细胞损伤或死亡的关键指标,LDH水平上升通常表明细胞活性下降或细胞受损。
在2D模型中,LDH水平在培养24小时后有所上升,48小时后略有下降。而人类皮肤活检样本的LDH水平逐日递增,培养48小时后几乎达到初始水平的3倍之多。相比之下,皮肤芯片展示出了明显的优势,其LDH水平在培养24小时后保持稳定,并在培养48小时后显著下降,显示出较好的细胞稳定性和长期培养潜力(图7),因此在长期实验中更具适用性。
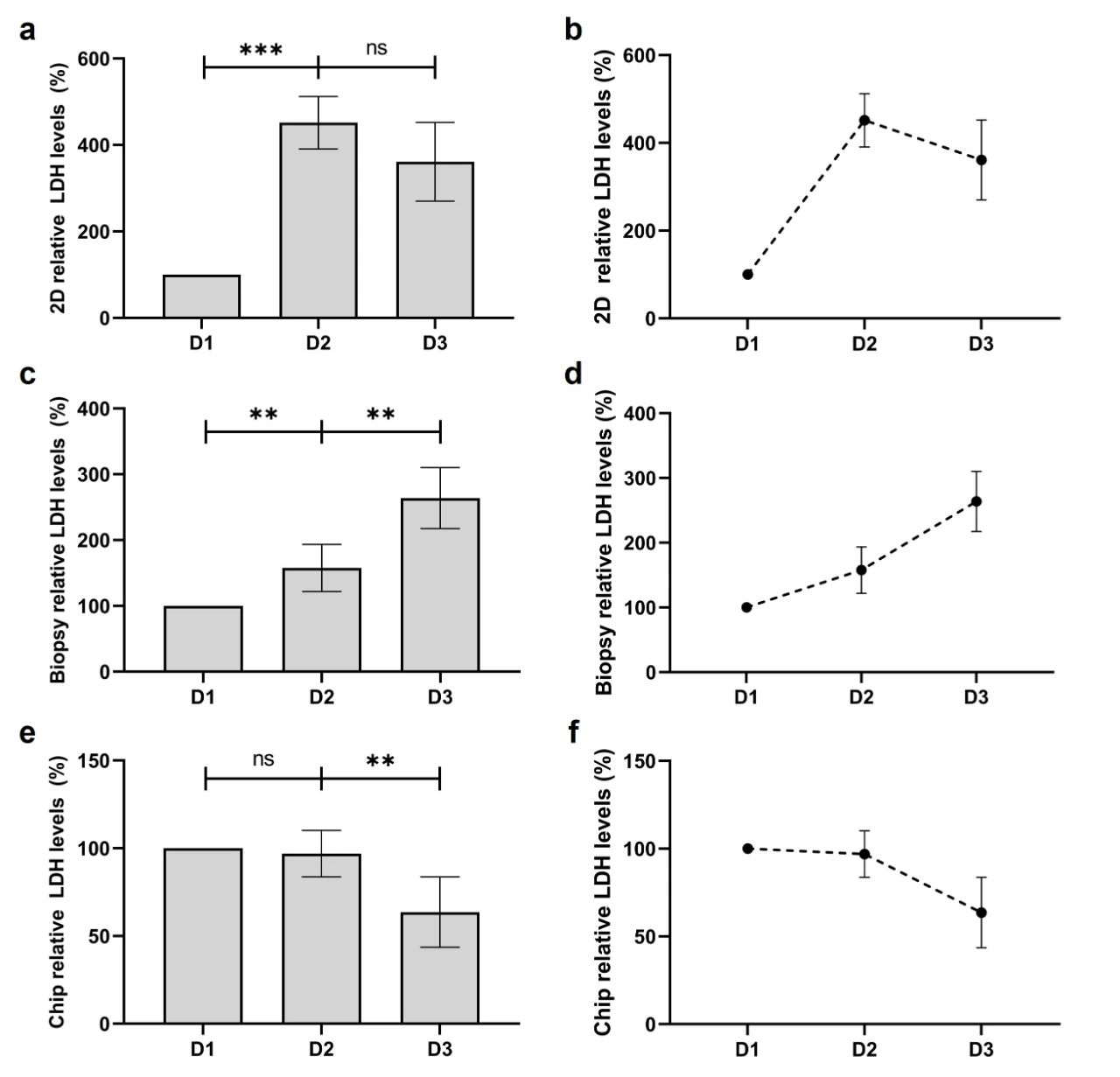
图7. 在3天培养过程中,不同模型中乳酸脱氢酶(LDH)的表达水平变化。(a,b) 2D单层培养中LDH的表达水平变化;(c,d) 人类皮肤活检样本中LDH的表达水平变化;(e,f) 皮肤芯片中的LDH的表达水平变化,LDH水平上升表明细胞活性下降或细胞受损。
06发展与期望,摩方持续推动终端应用发展
本研究开发的皮肤芯片结合了摩方精密的高精度3D打印技术与微流控系统,为药物与化妆品筛选提供了一个高度准确且具有生理相关性的体外模型。因此,该皮肤芯片通过与更多种类的药物和活性化合物相结合,有望为未来的生物医药和化妆品研究提供更多可能性。
总体而言,该皮肤芯片的开发标志着组织工程与药物测试技术的重大进展。通过提供一个更精准且用户友好的模型,使得摩方精密可以实现模拟人类皮肤的真实反应,并在皮肤科、药理学及化妆品研究中展现出巨大潜力。未来的研究将进一步整合更多类型的细胞,如灌注免疫细胞,以提升模型的应用性,并深入研究皮肤与免疫系统之间的相互作用,这一进展将有望为银屑病、湿疹及过敏反应等疾病的理解和治疗提供新思路。
原文链接:https://doi.org/10.3390/bioengineering11111055