在生命科学领域,真正困难的从来不是让细胞生长,而是让它们在三维空间中形成稳定而复杂的组织结构。对于培养肉技术而言,这一挑战尤为突出:当细胞规模不断扩大时,如何为组织内部持续输送氧气与营养,成为限制其发展的核心瓶颈。
近期,日本东京大学竹内昌治教授团队在这一问题上取得重要突破。研究人员成功构建了一种能够模拟生物血管系统的细胞培养平台,使肌肉细胞能够在厘米级厚度的三维结构中持续生长,并最终形成具有真实组织结构的鸡肉样组织。凭借这一创新成果,该研究入选《时代》周刊2025年度300项最佳发明榜,成为当年最受关注的生物技术创新之一。
在这一突破背后,高精度微结构制造发挥了关键作用。研究团队利用摩方精密微纳3D打印系统制造的结构组件,构建出用于固定与引导中空纤维的精密阵列,使人工血管网络能够在微米级尺度下精准搭建,从而为细胞组织提供稳定而均匀的营养供给环境。这一跨越生物工程与精密制造的技术融合,不仅推动培养肉研究迈向更真实的三维组织构建阶段,也展示了微纳级制造技术在生命科学前沿研究中的重要价值。

中空纤维生物反应器:构建“人工血管系统”
此前,培养肉技术面临的真正瓶颈并非启动细胞生长,而是如何让它们在三维空间中持续、健康地存活与增殖。在自然界,生物体依靠复杂绵密的毛细血管网络,将氧气与养分输送到每一个细胞,并将代谢废物运走。但在实验室的静态培养环境中,营养物质仅能通过扩散渗透,超过一定距离后组织中心的细胞便会因“窒息”和饥饿而迅速坏死,最终,人造肉类只能沦为一团无结构的“细胞糊”。
东京大学竹内昌治教授团队将目光投向了医学领域早已成熟的技术——中空纤维。他们将数根直径仅约0.3毫米、仿若发丝的半透性中空纤维,如同构建一套微型“人工血管”网络,三维嵌入到肌肉细胞中。通过在纤维内部持续灌注营养液,实现了对周围细胞的直接、均匀供养,从而让厘米级厚度的肌肉组织整体生长成为可能。这套中空纤维生物反应器系统(HFB),完美模拟了天然血管系统的核心功能,一举突破了组织工程中最大的尺寸限制。
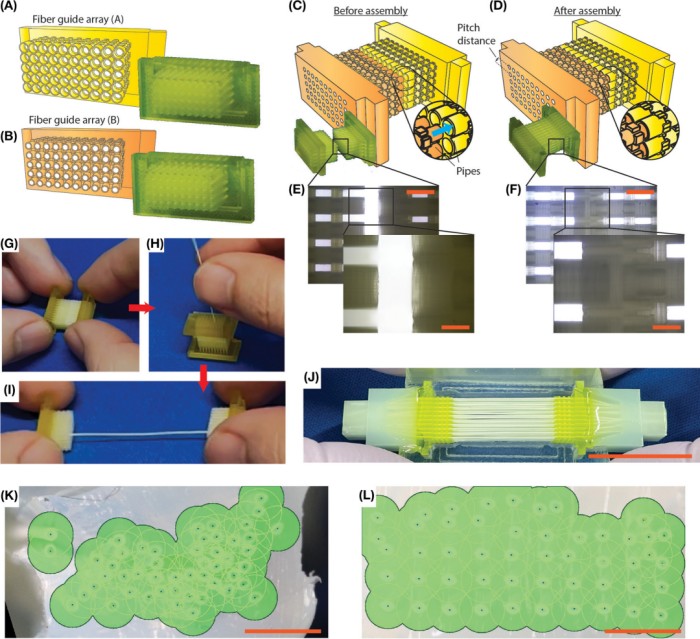
图1. HFB成功培养出的厘米级鸡肉组织的结构和过程。
微纳3D打印:构建精密纤维导向阵列的关键技术
然而,这一构想的真正挑战在于工程实现。中空纤维直径极小,需要在三维空间中按照精确间距进行排列,并保持稳定结构。同时,纤维之间的排列还必须支持细胞定向生长,使其形成类似天然肌肉的纤维结构。
为实现这一复杂结构,研究团队设计了两组高精度纤维导向阵列。这些结构包含精密的孔洞与微型凹槽,可在微米级精度下固定每一根中空纤维的位置。更重要的是,这些阵列表面还设计了特殊的微结构锚定点,用于引导细胞沿既定方向排列,从而形成具有真实纹理的肌肉纤维组织。
这些关键组件正是由摩方精密 microArch® S140 微纳3D打印系统制造完成。该设备具备10微米级制造精度,能够快速构建复杂的微尺度结构,为纤维网络的精准定位与稳定支撑提供了可靠的制造基础。
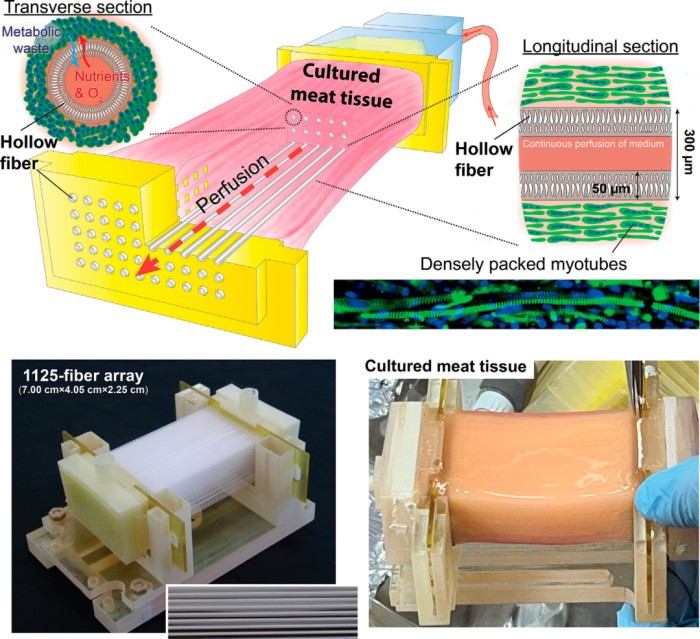
图2. 利用摩方精密微纳3D打印技术和中空纤维设计制造了HFB。
东京大学团队以创新思维提出了解决方案,而摩方精密的微纳3D打印技术,则将这些复杂结构精准制造出来,使实验设计能够稳定运行。从细胞机器人到培养肉,再到未来更复杂的生物组织制造,微纳级精密制造正在成为连接科学构想与现实应用的重要桥梁。
当实验室中的一块“鸡肉”跻身《时代》年度最佳发明榜时,它不仅代表食品科技的一次跃迁,也折射出一个更深层的趋势,即先进制造技术正在不断拓展科学研究的边界。