癌症免疫治疗的核心在于激活人体自身的免疫系统来识别和杀灭肿瘤细胞,而树突状细胞(DC)作为最重要的专职抗原呈递细胞,能够有效介导固有免疫应答并激活适应性免疫,其功能状态还决定了免疫应答的强度与质量,因而在抗肿瘤免疫中处于核心地位。近年来研究发现,NLRP3炎性小体的激活可以诱导DC进入一种"超激活"的特殊状态,超激活DC不同于NLRP3激活通常导致的细胞焦亡,能够在分泌白细胞介素-1β的同时保持细胞活力,并上调共刺激分子表达,兼具更高效的抗原呈递能力和更强的迁移能力,是促进CD8+ T细胞免疫应答的理想DC表型。然而,目前的DC超激活诱导方案仍普遍存在启动信号安全性不足、激活信号组成复杂、刺激强度难以调控等问题,从而限制了其在肿瘤疫苗中的进一步应用。
针对以上问题,中国科学院上海硅酸盐研究所陈航榕研究员、马明研究员团队构建了脂肪酸修饰并负载质粒DNA(pDNA)的脂质纳米颗粒(FA-pLNP)平台。其中,pDNA可编码肿瘤抗原并提供NF-κB介导的NLRP3炎症小体启动信号;脂肪酸提供炎症小体的激活信号,并通过调节信号强度实现了对DC超激活状态的可控诱导。相关成果以"Combinatorial Design of Fatty Acid-Incorporated Plasmid Lipid Nanoparticles Drives Dendritic Cell Hyperactivation for Enhanced Cancer Immunotherapy"为题发表在《ACS Nano》上。
本研究以FDA批准的疫苗脂质组成与比例作为基准配方,引入四种不同碳链长度及饱和度的脂肪酸,分别按五个摩尔比梯度掺入,构建了包含20种候选配方的FA-pLNP库。以DC成熟度为筛选指标,最终筛选得到最优配方——掺入15%棕榈酸的pLNP(命名为PA15)。
本研究基于团队自主开发的螺旋聚焦流微混合器,实现了优选脂质纳米颗粒PA15的稳定可控制备。该微混合器采用摩方精密面投影微立体光刻(PμSL)3D打印技术(nanoArch® S140,精度:10 μm),一体化成型出具有3D同轴聚焦螺旋通道的复杂结构。含有脂质的乙醇溶液与含pDNA的水溶液分别从独立入口注入,在螺旋通道内流动并进入混合区,两相流体快速混合,促使脂质与pDNA在毫秒级时间内完成自组装,从而获得粒径更均一的纳米颗粒。此外,团队以螺旋聚焦流微混合器为核心,开发了螺旋聚焦流纳米药物合成仪。该仪器配备触屏数显界面、微混合器连接件及自动收集台,具有批次间高重复性、操作简便等优势,适用于纳米脂质体、脂质纳米颗粒等多种纳米颗粒的高流速、均一化合成。
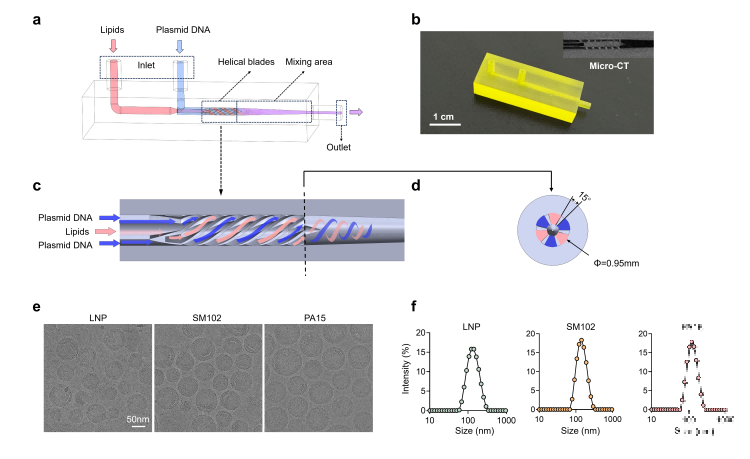
图.(a)螺旋聚焦流微混合器装置示意图;(b)装置实物照片及核心混合区的显微CT图像;(c)混合区内流动模式示意图;(d)螺旋通道出口处的横截面视图;(e)三种不同配方获得的脂质纳米颗粒的冷冻透射电镜图像;(f)通过动态光散射测得不同类型脂质纳米颗粒的水合动力学粒径分布。
进一步研究证实,在B16-OVA和MC38两种小鼠肿瘤模型中,PA15显著增强DC成熟与抗原呈递,能从数量(增加比例)、质量(增强功能)和空间分布(促进浸润)三个维度全面诱导强效的CD8⁺ T细胞应答,肿瘤生长抑制率分别达到91.7%和74.1%。上述发现为癌症疫苗及相关免疫治疗的研究提供了新的思路。
上述研究成果系中国科学院上海硅酸盐研究所与国科大杭州高等研究院的科研人员共同完成,研究生李孜印和贾福浩为共同第一作者,马明研究员和陈航榕研究员为共同通讯作者。
原文链接:https://doi.org/10.1021/acsnano.6c01946